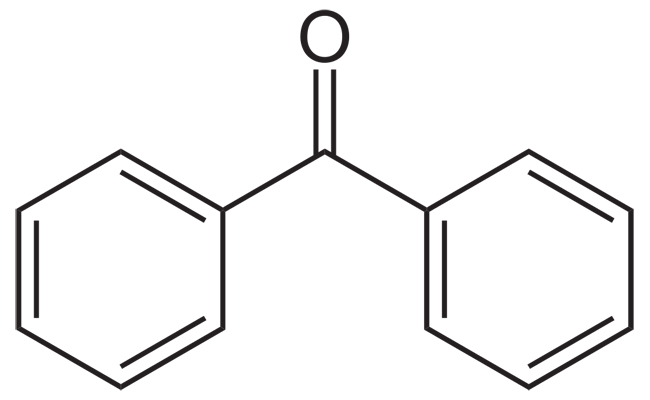
بنزوفنون چیست ؟
بنزوفنون Benzophenone با فرمول شیمیایی C۱۳H۱۰O یک ترکیب شیمیایی با شناسه پابکم ۳۱۰۲ است.
شکل ظاهری بنزوفنون جامد سفید است.
بنزوفنون یک ماده ارگانیک است که به طور طبیعی در میوه ها به خصوص در انگور یافت می شود.
بنزوفنون ماده ای طعم دهنده است.
بنزوفنون به علت اینکه در برابر اشعه ماورابنفش مقاوم است در بسیاری از فرمولاسیون های مراقبت پوستی مورد استفاده قرار می گیرد.
بنزوفنون به عنوان واسطه جاذب اشعه ماورابنفش در رنگدانه های آلی، داروها و عطر و حشره کش استفاده می شود.