سری الکتروشیمیایی چیست؟
یک سری الکتروشیمیایی که به عنوان سری نیروی الکتروموتیو (EMF) یا سری پتانسیل الکترود استاندارد نیز شناخته میشود، فهرستی از فلزات و غیرفلزات است که به ترتیب واکنش نسبی یا تمایل آنها برای انجام واکنشهای اکسیداسیون یا کاهش مرتب شدهاند.
این یک رتبه بندی از مواد را بر اساس پتانسیل الکترودی استاندارد آنها ارائه می دهد، که نشان دهنده سهولت در بدست آوردن یا از دست دادن الکترون در واکنش های الکتروشیمیایی است.
نکات مهم درباره سری الکتروشیمیایی
سری الکتروشیمیایی معمولاً به صورت جدول یا نمودار نشان داده می شود که بیشترین عناصر فعال در یک انتها و کمترین عناصر راکتیو در سمت دیگر دارند.
الکترود هیدروژن استاندارد (SHE) اغلب به عنوان یک نقطه مرجع استفاده می شود و یک پتانسیل الکترود استاندارد دلخواه صفر ولت اختصاص می دهد. پتانسیل الکترود سایر مواد نسبت به الکترود هیدروژن اندازه گیری می شود.
در سری الکتروشیمیایی، عناصر یا موادی که پتانسیل الکترودی بالاتری نسبت به هیدروژن دارند، بیشتر تحت احیاء (به دست آوردن الکترون) قرار می گیرند و به عنوان عوامل اکسید کننده عمل می کنند.
از سوی دیگر، عناصر یا موادی با پتانسیل الکترودی کمتر از هیدروژن بیشتر تحت اکسیداسیون (از دست دادن الکترون ها) قرار می گیرند و به عنوان عوامل کاهنده عمل می کنند.

سری الکتروشیمیایی در پیشبینی امکانسنجی و جهت واکنشهای ردوکس مفید است. با مقایسه پتانسیل های الکترود دو ماده، می توان تعیین کرد که در یک سلول یا واکنش الکتروشیمیایی مشخص، کدام ماده اکسید شده و کدام ماده کاهش می یابد. هرچه اختلاف پتانسیل الکترود بین دو ماده بیشتر باشد، نیروی محرکه برای واکنش ردوکس بیشتر است.
سری الکتروشیمیایی همچنین به درک رفتار فلزات در محیط های مختلف مانند تمایل آنها به خوردگی یا سازگاری آنها در سلول های گالوانیکی کمک می کند. فلزات بالاتر در این سری بیشتر در معرض خوردگی هستند، در حالی که فلزات در سری پایین تر در برابر خوردگی مقاوم تر هستند.
توجه به این نکته مهم است که سری های الکتروشیمیایی روند کلی واکنش پذیری را ارائه می دهند، اما سرعت و نتایج واقعی واکنش می تواند تحت تأثیر عوامل دیگری مانند غلظت، دما و وجود کاتالیزورها یا بازدارنده ها باشد.
واکنشهای ردوکس:
سری الکتروشیمیایی مبتنی بر اصول واکنشهای ردوکس (کاهش-اکسیداسیون) است.
واکنشهای ردوکس شامل انتقال الکترونها بین گونهها است، جایی که یک گونه تحت کاهش (الکترون به دست میآورد) و دیگری تحت اکسیداسیون (الکترونها را از دست میدهد).
سری الکتروشیمیایی به تعیین جهت انتقال الکترون و قدرت نسبی عوامل اکسید کننده و کاهنده کمک می کند.
پتانسیلهای الکترود استاندارد:
پتانسیل های الکترود ذکر شده در سری الکتروشیمیایی، پتانسیل های الکترود استاندارد هستند که اغلب با E° نشان داده می شوند.
این مقادیر در شرایط استاندارد اندازه گیری می شوند که شامل غلظت 1 مول در لیتر، دمای 25 درجه سانتیگراد و فشار 1 اتمسفر می باشد. پتانسیل های الکترود استاندارد یک مرجع ثابت برای مقایسه واکنش پذیری مواد مختلف فراهم می کند.
موقعیت در سری:
موقعیت یک ماده در سری الکتروشیمیایی نشان دهنده تمایل نسبی آن به کاهش یا اکسید شدن است.
مواد بالاتر در سری تمایل بیشتری به کاهش دارند (به عنوان عوامل اکسید کننده عمل می کنند)، در حالی که مواد پایین تر در سری تمایل بیشتری به اکسید شدن دارند (به عنوان عوامل کاهنده عمل می کنند). به عنوان مثال، فلزاتی مانند لیتیوم و پتاسیم بسیار واکنش پذیر هستند و جایگاه بالاتری در سری دارند، در حالی که فلزات نجیب مانند طلا و پلاتین واکنش کمتری دارند و موقعیت پایین تری دارند.
واکنشهای نیمه سلولی:
سری الکتروشیمیایی از مشاهده واکنش های نیمه سلولی به دست می آید. هر ورودی در این سری یک نیم سلول متشکل از یک فلز یا یک گونه در حالت استاندارد و یک یون مربوطه در محلولی از یون های آن را نشان می دهد.
پتانسیل استاندارد الکترود یک نیم سلول با اتصال آن به یک الکترود مرجع، مانند الکترود هیدروژن استاندارد، و اندازه گیری اختلاف پتانسیل اندازه گیری می شود.
پیش بینی خودانگیختگی:
سری الکتروشیمیایی به پیش بینی خود به خودی واکنش های ردوکس کمک می کند. اگر ماده بالاتر در سری در تماس با ماده پایینتر سری قرار گیرد، واکنش احتمالاً خود به خود ادامه مییابد و ماده بالاتر به عنوان عامل اکسید کننده و ماده پایینتر به عنوان عامل کاهنده عمل میکند.
هرچه اختلاف پتانسیل های الکترود بیشتر باشد، واکنش مطلوب تر است.
خوردگی و سلولهای گالوانیکی:
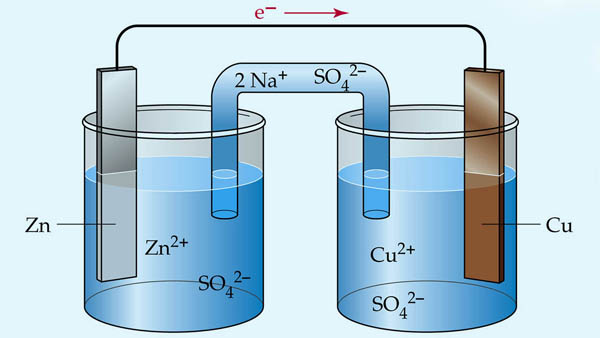
سری الکتروشیمیایی بینشی در مورد رفتار خوردگی و سازگاری فلزات در سلول های گالوانیکی ارائه می دهد. فلزات بالاتر در این سری زمانی که در معرض الکترولیت قرار می گیرند بیشتر دچار خوردگی می شوند، در حالی که فلزات سری پایین تر در برابر خوردگی مقاوم تر هستند. در یک سلول گالوانیکی، سری الکتروشیمیایی به تعیین جهت جریان الکترون و نیروی الکتروموتیو (EMF) تولید شده کمک می کند.
کاربرد در باتریها و الکترولیز:
سری الکتروشیمیایی در طراحی و عملکرد باتری ها مانند تعیین مواد آند و کاتد استفاده می شود. همچنین در فرآیندهای الکترولیز، که در آن از الکتریسیته برای هدایت واکنشهای ردوکس غیر خود به خودی استفاده میشود، مرتبط است. سری الکتروشیمیایی به انتخاب مواد الکترود مناسب برای الکترولیز کمک می کند.
توجه به این نکته مهم است که سری الکتروشیمیایی رتبه بندی ساده ای از واکنش پذیری را ارائه می دهد و بر اساس شرایط استاندارد است. شرایط دنیای واقعی، مانند غلظتهای مختلف، دما و وجود ناخالصیها، میتوانند بر رفتار واقعی واکنشهای ردوکس تأثیر بگذارند. با این وجود، سری الکتروشیمیایی ابزار ارزشمندی برای درک و پیشبینی رفتار مواد در فرآیندهای الکتروشیمیایی باقی میماند.